निर्जलीकरण अभिक्रिया
रसायन विज्ञान में निर्जलीकरण अभिक्रिया (अंग्रेज़ी: Dehydration reaction) एक रासायनिक अभिक्रिया है जिसमें अभिक्रिया करने वाले अणु या आयन से पानी की ह्रास शामिल होती है। निर्जलीकरण अभिक्रियायें सामान्य प्रक्रियाएँ हैं जो जलयोजन अभिक्रिया के विपरीत होती हैं।
कार्बनिक रसायन विज्ञान में निर्जलीकरण अभिक्रियायें
एस्टरीकरण
फिशर एस्टरीकरण निर्जलीकरण अभिक्रिया का उत्कृष्ट उदाहरण है, जिसमें एस्टर बनाने के लिए कार्बोक्सिलिक अम्ल को अल्कोहल के उपयोग किया जाता है।
- RCO2H + R′OH
 RCO2R′ + H2O
RCO2R′ + H2O
अक्सर ऐसी अभिक्रियाओं के लिए निर्जलनकर्मक की उपस्थिति की आवश्यकता होती है, यानी एक ऐसा पदार्थ की आवश्यकता होती जो पानी के साथ अभिक्रिया करता है।
ईथरीकरण
ग्लूकोज और फल शर्करा जैसे दो एकलशर्करा को निर्जलीकरण संश्लेषण का उपयोग करके एक साथ जोड़ा (सूक्रोज) बनाया जा सकता है। दो एकलशर्करा से युक्त नए अणु को डाइसैकेराइड कहा जाता है।
नाइट्राइल का निर्माण
नाइट्राइल्स अक्सर प्राथमिक एमाइड्स के निर्जलीकरण द्वारा तैयार किए जाते हैं।
- RC(O)NH2 → RCN + H2O
केटीन का निर्माण
केटीन एसीटिक अम्ल को गर्म करने और उत्पाद को विपाशन से उत्पन्न होता है।[1]
- CH3CO2H → CH2=C=O + H2O
एल्कीन का निर्माण
निर्जलीकरण द्वारा एल्कोहल से एल्कीन बनाया जा सकता है। इस रूपांतरण का उपयोग अन्य चीजों के अलावा, बायोमास को तरल ईंधन में परिवर्तित करने में किया जाता है।[2] इथेनॉल का एथिलीन में रूपांतरण एक मौलिक उदाहरण है,[3][4]
- CH3CH2OH → H2C=CH2 + H2O
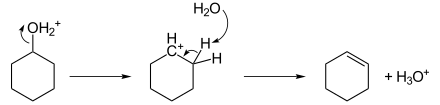
अभिक्रिया को अम्ल उत्प्रेरक जैसे सल्फ्यूरिक अम्ल और कुछ जिओलाइट द्वारा त्वरित किया जाता है। ये अभिक्रियाएं अक्सर कार्बोकेशन]]आईसी मध्यवर्ती के माध्यम से आगे बढ़ती हैं जैसा कि साइक्लोहेक्सानॉल के निर्जलीकरण के लिए दिखाया गया है।[5]
कुछ अल्कोहल से निर्जलीकरण का खतरा होता है। 3-हाइड्रॉक्सिलकार्बोनिल, जिन्हें एल्डोलएस कहा जाता है, कमरे के तापमान पर खड़े होने पर पानी छोड़ते हैं।
- RC(O)CH2CH(OH)R' → RC(O)CH=CHR' + H2O
अभिक्रिया निर्जलीकरण अभिकर्मकों द्वारा प्रेरित होती है। उदाहरण के लिए, 2-मिथाइल-साइक्लोहेक्सन-1-ओएल मार्टिन सल्फ्यूरेन की उपस्थिति में 1-मिथाइलसाइक्लोहेक्सिन में निर्जलित हो जाता है, जो पानी के साथ अपरिवर्तनीय रूप से अभिक्रिया करता है।[6][7]
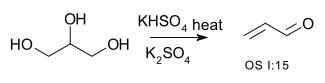
दोहरे निर्जलीकरण को ग्लिसरॉल से एक्रोलिन में परिवर्तित करके दर्शाया गया है,[8][9]
सन्दर्भ
- ↑ “उलमैन का औद्योगिक रसायनविज्ञान ज्ञानकोश”।। (2001)। Weinheim: Wiley-VCH। DOI:10.1002/14356007.a15_063.
- ↑ Besson, Michèle; Gallezot, Pierre; Pinel, Catherine (2014-02-12). "Conversion of Biomass into Chemicals over Metal Catalysts". Chemical Reviews (अंग्रेज़ी में). 114 (3): 1827–1870. PMID 24083630. आइ॰एस॰एस॰एन॰ 0009-2665. डीओआइ:10.1021/cr4002269.
- ↑ Zimmermann, Heinz; Walz, Roland (2008). "Ethylene". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. आई॰ऍस॰बी॰ऍन॰ 978-3527306732. डीओआइ:10.1002/14356007.a10_045.pub3.
- ↑ Zhang, Minhua; Yu, Yingzhe (2013-07-17). "Dehydration of Ethanol to Ethylene". Industrial & Engineering Chemistry Research (अंग्रेज़ी में). 52 (28): 9505–9514. आइ॰एस॰एस॰एन॰ 0888-5885. डीओआइ:10.1021/ie401157c.
- ↑ G. H. Coleman, H. F. Johnstone (1925). "Cyclohexene". Organic Syntheses. 5: 33. डीओआइ:10.15227/orgsyn.005.0033.
- ↑ J. Brent Friesen; Robert Schretzman (2011). "Dehydration of 2-Methyl-1-cyclohexanol: New Findings from a Popular Undergraduate Laboratory Experiment". J. Chem. Educ. 88 (8): 1141–1147. डीओआइ:10.1021/ed900049b. बिबकोड:2011JChEd..88.1141F.
- ↑ Roden, Brian A. (2001). "Diphenylbis(1,1,1,3,3,3-hexafluoro-2-phenyl-2-propoxy)sulfurane". Encyclopedia of Reagents for Organic Synthesis. आई॰ऍस॰बी॰ऍन॰ 0471936235. डीओआइ:10.1002/047084289X.rd409.
- ↑ साँचा:OrgSynth
- ↑ Katryniok, Benjamin; Paul, Sébastien; Bellière-Baca, Virginie; Rey, Patrick; Dumeignil, Franck (2010). "Glycerol dehydration to acrolein in the context of new uses of glycerol". Green Chemistry (अंग्रेज़ी में). 12 (12): 2079. आइ॰एस॰एस॰एन॰ 1463-9262. डीओआइ:10.1039/c0gc00307g.