1,1,1-ट्राइक्लोरोइथेन
| १,१,१-ट्राईक्लोरोईथेन | |
|---|---|
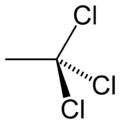 |  |
| आईयूपीएसी नाम | 1,1,1-trichloroethane |
| अन्य नाम | मिथाइल क्लोरोफ़ॉर्म, क्लोरोथीन, सॉल्वेन्ट १११,जेन्क्लीन, R-140a |
| पहचान आइडेन्टिफायर्स | |
| सी.ए.एस संख्या | [71-55-6][CAS] |
| पबकैम | |
| केईजीजी | C18246 |
| रासा.ई.बी.आई | 36015 |
| SMILES | |
| InChI | |
| कैमस्पाइडर आई.डी | |
| गुण | |
| आण्विक सूत्र | C2H3Cl3 या CH3CCl3 |
| मोलर द्रव्यमान | 133.40 ग्रा/मोल |
| दिखावट | वर्णहीन तरल |
| गंध | सौम्य, क्लोरोफ़ॉर्म जैसा[3] |
| घनत्व | 1.32 ग्रा/सेंमी3 |
| गलनांक | -33 °C, 240 K, -27 °F |
| क्वथनांक | 74 °C, 347 K, 165 °F |
| जल में घुलनशीलता | 0.4% (20°से)[3] |
| वाष्प दबाव | 100 मिमिHg (20 °C)[3] |
| खतरा | |
| Main hazards | Irritant to the upper respiratory tract. Causes severe irritation and swelling to eyes. |
| NFPA 704 |  1 3 1 |
| Explosive limits | 7.5%-12.5%[3] |
| यू.एस अनुज्ञेय अवस्थिति सीमा (पी.ई.एल) | TWA 350 ppm (1900 mg/m3)[3] |
| एलडी५० | 9600 mg/kg (oral, rat) 6000 mg/kg (oral, mouse) 5660 mg/kg (oral, rabbit) [4] |
| जहां दिया है वहां के अलावा, ये आंकड़े पदार्थ की मानक स्थिति (२५ °से, १०० कि.पा के अनुसार हैं। | |
1,1,1-ट्राइक्लोरोइथेन एक कार्बनिक यौगिक है।
1,1,1-ट्राइक्लोरोइथेन को तैयार करने की विधि
1,1,1-ट्रिक्लोरोइथेन पहली बार 1840 में हेनरी विक्टर रेगनाल्ट द्वारा रिपोर्ट किया गया था। औद्योगिक रूप से, यह आमतौर पर vinyl chloride से दो-चरण की प्रक्रिया में निर्मित होता है। पहले चरण में, vinyl chloride 1,1-dichloroethane का उत्पादन करने के लिए 20-50 डिग्री सेल्सियस पर hydrogen chloride के साथ प्रतिक्रिया करता है:
CH2=CHCl + HCl → CH3CHCl2
यह प्रतिक्रिया विभिन्न प्रकार के लुईस एसिड से उत्पन्न होती है, मुख्य रूप से aluminium chloride, Fe (III) chloride या जस्ता क्लोराइड। पराबैंगनी विकिरण के तहत क्लोरीन के साथ प्रतिक्रिया से 1,1-dichloroethane को 1,1,1-ट्रिक्लोरोइथेन में परिवर्तित किया जाता है:
CH3CHCl2 + Cl2 → CH3CCl3 + HCl
80-90% उपज पर यह प्रतिक्रिया आय, और hydrogen chloride उप-उत्पाद प्रक्रिया में पहले चरण के लिए पुनर्नवीनीकरण किया जा सकता है। प्रमुख साइड-उत्पाद 1,2,2-trichloroethane से सम्बद्ध है, जिसमें से 1,1,1-ट्रिक्लोरोइथेन को आसवन द्वारा अलग किया जा सकता है।
Fe (III) chloride उत्प्रेरक की उपस्थिति में vinylidene chloride और hydrogen chloride की प्रतिक्रिया से 1,1,1-ट्रिक्लोरोइथेन की कुछ छोटी मात्रा का उत्पादन होता है:
CH2=CCl2 + HCl → CH3CCl3
1,1,1-ट्रिक्लोरोइथेन स्टेबलाइजर्स के साथ विपणन किया जाता है क्योंकि यह डीहाइड्रोक्लोरिनीकरण के संबंध में अस्थिर है और कुछ धातुओं पर हमला करता है। स्टेबलाइजर्स में एसिड स्केवेनर (एपॉक्साइड, एमाइंस) और कॉम्प्लेन्टस सहित 8% सूत्रीकरण शामिल हैं। ozone depletion के लिए जिम्मेदार उन यौगिकों में से एक के रूप में मॉन्ट्रियल प्रोटोकॉल को 1,1,1-ट्राईक्लोरोइथेन को लक्षित किया गया और 1996 में इसका प्रयोग शुरू करने पर प्रतिबंध लगा दिया गया। तब से, इसका निर्माण और उपयोग पूरे विश्व में समाप्त हो चुका है।
उपयोग
1,1,1-ट्रिक्लोरोइथेन को आम तौर पर एक गैर-ध्रुवीय विलायक माना जाता है। क्लोरीन परमाणुओं के अच्छे ध्रुवीकरण के कारण, यह जैविक यौगिकों के लिए एक बेहतर विलायक है जो हाक्सन जैसे हाइड्रोकार्बन में अच्छी तरह भंग नहीं करता। यह कई कार्बनिक पदार्थों के लिए एक उत्कृष्ट विलायक है और chlorinated hydrocarbon के कम से कम विषाक्त पदार्थों में से एक है। मॉन्ट्रियल प्रोटोकॉल से पहले, यह धातु के हिस्सों और circuit boards की सफाई के लिए व्यापक रूप से इस्तेमाल किया गया था, इलेक्ट्रॉनिक्स उद्योग में एक फोटोसिसेंट विलायक के रूप में, एक एरोसोल प्रणोदक के रूप में, एक काटने वाले तरल पदार्थ additive के रूप में और स्याही, पेंट, चिपकने वाले और अन्य के लिए विलायक के रूप में कोटिंग्स। 1,1,1-ट्रिक्लोरोइथेन का उपयोग एक insecticidal fumigant के रूप में भी किया जाता है। [5]
यह फोटोग्राफिक फिल्म (मूवी / स्लाइड / निगेटिव इत्यादि) के लिए मानक क्लीनर भी था। अन्य सामान्य रूप से उपलब्ध सॉल्वैंट्स पायस को नुकसान पहुंचाते हैं, और इस तरह इस आवेदन के लिए उपयुक्त नहीं हैं। मानक प्रतिस्थापन, फोरेन 141 बहुत कम प्रभावी है, और एक अवशेष छोड़ देता है। 1,1,1-ट्रिक्लोरोइथेन का प्रयोग तरल पदार्थ जैसे सुधार द्रव उत्पादों में पतले के रूप में किया गया था। इसके कई अनुप्रयोगों ने पहले कार्बन टेट्राक्लोराइड का उपयोग किया था (जो 1 9 70 में अमेरिकी उपभोक्ता उत्पादों में प्रतिबंधित था)। बदले में, 1,1,1-ट्रिक्लोरोइथेन स्वयं को अब प्रयोगशाला में अन्य सॉल्वैंट्स द्वारा प्रतिस्थापित किया जा रहा है। [6]
सन्दर्भ
- ↑ अ आ "संग्रहीत प्रति" (PDF). मूल से 18 मई 2017 को पुरालेखित (PDF). अभिगमन तिथि 22 अप्रेल 2017.
|access-date=में तिथि प्राचल का मान जाँचें (मदद) - ↑ "संग्रहीत प्रति". मूल से 22 अप्रेल 2017 को पुरालेखित. अभिगमन तिथि 22 अप्रेल 2017.
|access-date=, |archive-date=में तिथि प्राचल का मान जाँचें (मदद) - ↑ अ आ इ ई उ "NIOSH Pocket Guide to Chemical Hazards #0404". National Institute for Occupational Safety and Health (NIOSH).
- ↑ सन्दर्भ त्रुटि:
<ref>का गलत प्रयोग;IDLHनाम के संदर्भ में जानकारी नहीं है। - ↑ Methylchloroform data sheet Archived 2017-10-29 at the वेबैक मशीन, alanwood.net
- ↑ "Use of Ozone Depleting Substances in Laboratories. TemaNord 516/2003" (PDF). मूल (PDF) से 27 फ़रवरी 2008 को पुरालेखित. अभिगमन तिथि 29 अक्टूबर 2017.