हिलियम
| हिलियम / Helium रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | He |
| परमाणु संख्या: | 2 |
| रासायनिक शृंखला: | निष्क्रिय गैसें |
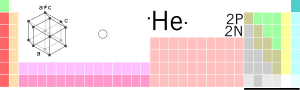 आवर्त सारणी में स्थिति | |
 | |
| अन्य भाषाओं में नाम: | Helium (अंग्रेज़ी) |


हिलियम (अंग्रेज़ी: Helium) एक रासायनिक तत्त्व है जो प्रायः गैसीय अवस्था में रहता है। यह एक निष्क्रिय गैस या नोबेल गैस (Noble gas) है तथा रंगहीन, गंधहीन, स्वादहीन, विष-हीन (नॉन-टॉक्सिक) भी है। इसका परमाणु क्रमांक २ है। सभी तत्वों में इसका क्वथनांक (boiling point) एवं गलनांक (melting point) सबसे कम है। द्रव हिलियम का प्रयोग पदार्थों को अत्यन्त कम ताप तक ठण्डा करने के लिये किया जाता है; जैसे अतिचालक तारों को १.९ डिग्री केल्विन तक ठण्डा करने के लिये।
हीलियम अक्रिय गैसों का एक प्रमुख सदस्य है। इसका संकेत He, परमाणुभार ४, परमाणुसंख्या २, घनत्व ०.१७८५, क्रांतिक ताप -२६७.९०० और क्रांतिक दबाव २ २६ वायुमंडल, क्वथनांक -२६८.९० सें. और गलनांक -२७२ डिग्री से. है। इसके दो स्थायी समस्थानिक He3, परमाण्विक द्रव्यमान ३.०१७० और He4, परमाण्विक द्रव्यमान ४.००३९ और दो अस्थायी समस्थानिक He5, परमाण्विक द्रव्यमान ५.०१३७ और रेडियोएक्टिव He6, परमाण्विक द्रव्यमान ६.०२८ पाए गए हैं। मेरा नाम बाबा है
खोज एवं प्राप्ति
१८६८ ई. में सूर्य के सर्वग्रास ग्रहण के अवसर पर सूर्य के वर्णमंडल के स्पेक्ट्रम में एक पीली रेखा देखी थी जो सोडियम की पीली रेखा से भिन्न थी। जानसेन ने इस रेखा का नाम डी3 रखा और सर जे. नार्मन लॉकयर इस परिणाम पर पहुँचे कि यह रेखा किसी ऐसे तत्व की है जो पृथ्वी पर नहीं पाया जाता। उन्होंने ही हीलियम (ग्रीक शब्द, शब्दार्थ सूर्य) के नाम पर इसका नाम हीलियम रखा। १८९४ ई. में सर विलियम रामजेम ने क्लीवाइट नामक खनिज से निकली गैस की परीक्षा से सिद्ध किया कि यह गैस पृथ्वी पर भी पाई जाती है। क्लीवाइट को तनु सल्फ्यूरिक अम्ल के साथ गरम करने और पीछे क्वीवाइट को निर्वात में गरम करने से इस गैस को प्राप्त किया था। ऐसी गैस में २० प्रतिशत नाइट्रोजन था। नाइट्रोजन के निकाल लेने पर गैस के स्पेक्ट्रम परीक्षण से स्पेक्ट्रम में डी3 रेखा मिली। पीछे पता लगा कि कुछ उल्कालोह में भी यह गैस विद्यमान थी। रामजे और टैवर्स ने इस गैस को बड़े परिश्रम और बड़ी सूक्ष्मता से परीक्षा कर देखा कि यह गैस वायुमंडल में भी रहता है। रामजे और फ्रेडेरिक सॉडी ने रेडियोऐक्टिव पदार्थों के स्वत:विघटन से प्राप्त उत्पाद में भी इस गैस को पाया। वायुमंडल में बड़ी अल्प मत्रा (१८,६०० में एक भाग), कुछ अन्य खनिजों, जैसे बोगेराइट और मोनेजाइट से निकली गैसों में यह पाया गया। मोनोज़ाइट के प्रति एक ग्राम में १ घन सेमी गैस पाई जाती है। पेट्रोलियम कूपों से निकली प्राकृतिक गैस में इसकी मात्रा १ प्रतिशत से लेकर ८ प्रतिशत तक पाई गई है।
उत्पादन
प्राकृतिक गैसों के धोने से कार्बन डाइआक्साइड और अन्य अम्लीय गैसें निकल जती हैं। धोने में मोनाइथेनोलेमिन और ग्लाइकोल मिला हुआ जल प्रयुक्त होता है। धोने के बाद गैस को सूखाकर उसे ग्र्क़ से ३०० डिग्री ताप तक ठंढा करते हैं। उस ताप पर प्रति वर्ग इंच ६०० पाउंड से अधिक दबाव डालते हैं। इससे हीलियम और कुछ नाइट्रोजन को छोड़कर अन्य सब गैसें तरलीभूत हो जाती हैं। अब हीलियम (५० प्रतिशत) और नाइट्रोजन (५०%) का मिश्रण बच जाता है। इसे और ठंडा कर प्रति वर्ग इंच २,५०० पाउंड दबाव से दबाते हैं जिससे अधिकांश नाइट्रोजन तरलीभूत हो जाता है और हीलियम की मात्रा ९८.२% तक पहुँच जाती है। यदि इससे अधिक शुद्ध हीलियम प्राप्त करना हो तो सक्रियकृत नारियल के कोयले को द्रव नाइट्रोजन के ऊष्मक में रखकर उसके द्वारा हीलियम को पारित करते हैं जिससे केवल लेशमात्र अपद्रव्यवाला हीलियम प्राप्त होता है।
गुणधर्म
वर्णरहित, गंधहीन और स्वादहीन गैस है। तापध्वनि और विद्युत का सुचालक है। जल में अल्प विलेय है। अन्य विलायकों में अधिक घुलता है। इसका तरलन हुआ है। द्रव हीलियम दो रूपों में पाया गया है। इसका घनत्व ०.१२२ है। इसका ठोसीकरण भी हुआ है। तरल द्रव के १४० वायुमंडल दबाव पर २७२ डिग्री से. पर कीसम ने १९२६ ई. में ठोस हीलियम प्राप्त किया था। इसकी गैस में केवल एक परमाणु रहता है। इसकी विशिष्ट ऊष्माओं का अनुपात ४ : १.६६७ है। किसी भी तत्व के साथ यह कोई यौगिक नहीं बनता। इसकी संयोजकता शून्य है। आवर्तसारणी में इसका स्थान प्रथम समूह के प्रबल विद्युत् धनीय तत्वों और सप्तम समूह के प्रबल विद्युत् ऋणीय तत्वों के बीच है।
उपयोग

वायु पोतों (airships) में हाइड्रोजन के स्थान में अब हीलियम का प्रयोग होता है यद्यपि हाइड्रोजन की तुलना में इसकी उत्थापक क्षमता ९२.६ प्रतिशत ही है पर हाइड्रोजन के ज्वलनशील होने और वायु के साथ विस्फोटक मिश्रण बनने के कारण अब हीलियम का ही उपयोग हो रहा है। मौसम का पता लगाने के लिए बैलूनों में भी हीलियम गैस का आज उपयोग होता है। हल्की धातुओं के जोड़ने और अन्य धातु कर्म संबंधी उपचारों में निष्क्रिय वायुमंडल के लिए हीलियम काम में आ रहा है। औषधियों में भी विशेषत: दमे और अन्य श्वसन रोगों में आक्सीजन के साथ मिलाकर कृत्रिम श्वसन में हीलियम का उपयोग बढ़ रहा है। द्रव हिलियम का प्रयोग पदार्थों को अत्यन्त कम ताप तक ठंड करने के लिए किया जाता है; जैसे अतिचालक तारों को १.९ डिग्री केल्विन तक ठंड करने के लिए।
इन्हें भी देखें
बाहरी कड़ियाँ
- The Periodic Table of Videos - Helium
- US Government' Bureau of Land Management: Sources, Refinement, and Shortage. With some History of Helium.
- U.S. Geological Survey Publicationson Helium beginning 1996
- It's Elemental – Helium
- विस्तृत जानकारी
- Helium at the Helsinki University of Technology; includes pressure-temperature phase diagrams for helium-3 and helium-4
- Lancaster University, Ultra Low Temperature Physics - includes a summary of some low temperature techniques
- विविध
- Physics in Speech with audio samples that demonstrate the unchanged voice pitch
- Article about helium and other noble gases
- Ebyte article on helium scarcity and potential effects on NMR and MRI communities