बेंजीन

| Benzene | |
|---|---|
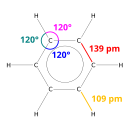 |  |
| बेंजीन अणु | |
| आईयूपीएसी नाम | बेंजीन (Benzene) |
| अन्य नाम | Benzol, Phene, Phenyl hydride |
| पहचान आइडेन्टिफायर्स | |
| सी.ए.एस संख्या | [71-43-2][CAS] |
| पबकैम | |
| EC संख्या | |
| केईजीजी | C01407 |
| रासा.ई.बी.आई | 16716 |
| RTECS number | CY1400000 |
| SMILES | |
| InChI | |
| कैमस्पाइडर आई.डी | |
| गुण | |
| रासायनिक सूत्र | C6H6 |
| मोलर द्रव्यमान | 78.11 g mol−1 |
| दिखावट | Colorless liquid |
| गंध | Aromatic, gasoline-like |
| घनत्व | 0.8765(20) g/cm3[1] |
| गलनांक | 5.53 °C, 279 K, 42 °F |
| क्वथनांक | 80.1 °C, 353 K, 176 °F |
| जल में घुलनशीलता | 1.53 g/L (0 °C) 1.81 g/L (9 °C) 1.79 g/L (15 °C)[2][3][4] 1.84 g/L (30 °C) 2.26 g/L (61 °C) 3.94 g/L (100 °C) 21.7 g/kg (200 °C, 6.5 MPa) 17.8 g/kg (200 °C, 40 MPa)[5] |
| घुलनशीलता | Soluble in alcohol, CHCl3, CCl4, diethyl ether, acetone, acetic acid[5] |
| ethanediol में घुलनशीलता | 5.83 g/100 g (20 °C) 6.61 g/100 g (40 °C) 7.61 g/100 g (60 °C)[5] |
| ethanol में घुलनशीलता | 20 °C, solution in water: 1.2 mL/L (20% v/v)[7] |
| acetone में घुलनशीलता | 20 °C, solution in water: 7.69 mL/L (38.46% v/v) 49.4 mL/L (62.5% v/v)[7] |
| diethylene glycol में घुलनशीलता | 52 g/100 g (20 °C)[5] |
| log P | 2.13 |
| वाष्प दबाव | 12.7 kPa (25 °C) 24.4 kPa (40 °C) 181 kPa (100 °C)[6] |
| रिफ्रेक्टिव इंडेक्स (nD) | 1.5011 (20 °C) 1.4948 (30 °C)[5] |
| श्यानता | 0.7528 cP (10 °C) 0.6076 cP (25 °C) 0.4965 cP (40 °C) 0.3075 cP (80 °C) |
| ढांचा | |
| आण्विक आकार | Trigonal planar |
| Dipole moment | 0 D |
| Thermochemistry | |
| फॉर्मेशन की मानक एन्थाल्पीΔfH | 48.7 kJ/mol |
| मानक मोलीय एन्ट्रॉपी S | 173.26 J/mol·K[6] |
| खतरा | |
| EU वर्गीकरण | साँचा:Hazchem F साँचा:Hazchem T Carc. Cat. 1 Muta. Cat. 2 |
| Main hazards | potential occupational carcinogen, flammable |
| NFPA 704 |  3 2 0 |
| R-फ्रेसेज़ | साँचा:R45, साँचा:R46, R11, साँचा:R16, R36/38,साँचा:R48/23/24/25, साँचा:R65 |
| S-फ्रेसेज़ | साँचा:S53, S45 |
| Explosive limits | 1.2–7.8% |
| यू.एस अनुज्ञेय अवस्थिति सीमा (पी.ई.एल) | TWA 1 ppm, ST 5 ppm[8] |
| एलडी५० | 930 mg/kg (rat, oral) |
| जहां दिया है वहां के अलावा, ये आंकड़े पदार्थ की मानक स्थिति (२५ °से, १०० कि.पा के अनुसार हैं। | |
बेंज़ीन या धूपेन्य एक हाइड्रोकार्बन है जिसका अणुसूत्र C6H6 है। बेंजीन का अणु ६ कार्बन परमाणुओं से बना होता है जो एक छल्ले की तरह जुड़े होते हैं तथा प्रत्येक कार्बन परमाणु से एक हाइड्रोजन परमाणु जुड़ा होता है।
बेंजीन, पेट्रोलियम (क्रूड ऑयल) में प्राकृतिक रूप से पाया जाता है। कोयले के शुष्क आसवन से अलकतरा तथा अलकतरे के प्रभाजी आसवन (fractional distillation) से बेंजीन बड़ी मात्रा में तैयार होता है। प्रदीपन गैस से प्राप्त तेल से फैराडे ने 1825 ई॰ में सर्वप्रथम इसे प्राप्त किया था। मिटशरले ने 1834 ई॰ में बेंज़ोइक अम्ल से इसे प्राप्त किया और इसका नाम बेंजीन रखा। अलकतरे में इसकी उपस्थिति का पता पहले पहल 1845 ई॰ में हॉफमैन (Hoffmann) ने लगाया था। जर्मनी में बेंजीन को 'बेंज़ोल' कहते हैं।
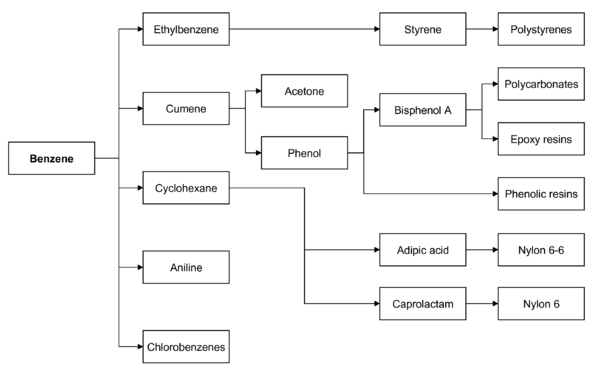
बेंजीन रंगहीन, मीठी गन्थ वाला, अत्यन्त ज्वलनशील द्रव है। इसका उपयोग एथिलबेंजीन्न और क्यूमीन (cumene) आदि भारी मात्रा में उत्पादित रसायनों के निर्माण में होता है। चूँकि बेंजीन का ऑक्टेन संख्या अधिक होती है, इसलिये पेट्रोल में कुछ प्रतिशत तक यह मिलाया गया होता है। यह कैंसरजन है जिसके कारण इसका गैर-औद्योगिक उपयोग कम ही होता है।
गुण
धूपेन्य प्रांगार और उदजन का एक यौगिक, हाइड्रोकार्बन, है। यह वर्णहीन और प्रबल अपवर्तक द्रव है। इसका क्वथनांक 80 डिग्रीसें॰, ठोस बनने का ताप 5.5 डिग्रीसें॰ और घनत्व 0 डिग्रीसें॰ पर 0.899 है। इसकी गंध ऐरोमैटिक और स्वाद विशिष्ट होता है। जल में यह बड़ा अल्प विलेय, सुषव में अधिक विलेय तथा ईथर और कार्बन डाइसल्फाइड में सब अनुपातों में विलेय है। विलायक के रूप में रबर, गोंद, वस, गंधक और रेज़िन के घुलाने में प्रचुरता से प्रयुक्त होता है। जलते समय इससे धुंआँ निकलता है। रसायनत: यह सक्रिय होता है। नीरजी से दो प्रकार का यौगिक बनता है : एक योगशील और दूसरा प्रतिस्थापित यौगिक। गन्धकाम्ल से धूपेन्य गन्धकाम्ल, भूयिकाम्ल (नाइट्रिक अम्ल) से भूया (नाइट्रो) धूपेन्य और ओज़ोन से धूपेन्य ट्राइओज़ोनाइड, [C6H6 (O3)3] बनता है। अवकरण से धूपेन्य साइक्लो हेक्सेन बनता है।
विलायक के अतिरिक्त, धूपेन्य बड़ी मात्रा में ऐनिलीन, कृत्रिम प्रक्षालक, कृमिनाशक, डी॰डी॰टी॰, दर्शव (जिससे प्लास्टिक बनते हैं), इत्यादि के निर्माण में प्रयुक्त होता है। मोटर इंजन के लिए पेट्रोल में कुछ धूपेन्य मिलाने से पेट्रोल की उत्कृष्टता बढ़ जाती है।
संरचना
बेंजीन में छह कार्बन परमाणु और छह हाइड्रोजन परमाणु हैं, अत: इसका अणुसूत्र (C6H6) है। केकूले ने 1865 ई॰ में पहले पहल सिद्ध किया कि इसके छह कार्बन परमाणु एक वलय के रूप में विद्यमान हैं, जिसको धूपेन्य वलय की संज्ञा दी गई है। प्रत्येक कार्बन परमाणु एक बंध से हाइड्रोजन से और दो से अन्य निकटवर्ती कार्बन परमाणुओं से संबद्ध रहता है। कार्बन का चौथा बंध युग्म बंध के रूप में उपस्थित माना गया है। ऐसे संरचनासूत्र से बेंज़ोन के गुणों की व्याख्या बड़ी सरलता से हो जाती है। ऊपर दिया हुआ यह सूत्र प्राय: सर्वमान्य है।
बेंजीन के विभिन्न प्रस्तावित संरचनात्मक सूत्र 




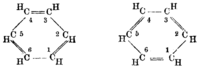
Von Adolf Karl Ludwig Claus (1867) Von James Dewar (1867) Von Albert Ladenburg (1869) Von Henry Edward Armstrong (1887),
Adolf von Baeyer (1888)Von Friedrich Karl Johannes Thiele (1899) Von August Kekulé (1872)
बेंजीन की प्राप्ति के लिए अलकतरे को इस्पात के भभकों में आसुत करते हैं। जो आसुत 90 डिग्री सें. और 170 डिग्री सें. के बीच प्राप्त होता हे, उसे हल्का तेल कहते हैं। पानी से हलका होने के कारण यह हल्का कहा है। हल्के तेल को पहले सोडियम हाइड्रॉक्साइड के जलीय विलयन जाता से धोकर अम्लों को निकाल लेते हैं। फिर सांद्र सल्फ्यूरिक अम्ल से धोकर क्षारों को निकाल लेते हैं। इसके बाद प्रभाजी स्तंभ की सहायता से प्रभाजन कर धूपेन्य को पृथक् करते हैं। यही व्यापार का धूपेन्य है। इसमें अब भी कुछ अपद्रव्य, थायोफीन और अन्य हाइड्रोकार्बन मिले रहते हैं। सांद्र सल्फ्यूरिक अम्ल द्वारा उपचार के बाद उत्पाद के क्रिस्टलीकरण से शुद्ध धूपेन्य प्राप्त होता है।
बाहरी कड़ियाँ
- International Chemical Safety Card 0015
- USEPA Summary of Benzene Toxicity
- NIOSH Pocket Guide to Chemical Hazards
- साँचा:PubChemLink
- Dept. of Health and Human Services: TR-289: Toxicology and Carcinogenesis Studies of Benzene
- Video Podcast of Sir John Cadogan giving a lecture on Benzene since Faraday, in 1991
- Substance profile
- U.S. National Library of Medicine: ChemIDplus - Benzene
- NLM Hazardous Substances Databank – Benzene
- ↑ साँचा:RubberBible86th
- ↑ Arnold, D.; Plank, C.; Erickson, E.; Pike, F. (1958). "Solubility of Benzene in Water". Industrial & Engineering Chemistry Chemical & Engineering Data Series. 3 (2): 253–256. डीओआइ:10.1021/i460004a016.
- ↑ Breslow, R.; Guo, T. (1990). "Surface tension measurements show that chaotropic salting-in denaturants are not just water-structure breakers". Proceedings of the National Academy of Sciences of the United States of America. 87 (1): 167–9. PMID 2153285. डीओआइ:10.1073/pnas.87.1.167. पी॰एम॰सी॰ 53221. बिबकोड:1990PNAS...87..167B.
- ↑ Coker, A. Kayode; Ludwig, Ernest E. (2007). Ludwig's Applied Process Design for Chemical And Petrochemical Plants. 1. Elsevier. पृ॰ 114. आई॰ऍस॰बी॰ऍन॰ 0-7506-7766-X. मूल से 12 मार्च 2016 को पुरालेखित. अभिगमन तिथि 2012-05-31.
- ↑ अ आ इ ई उ "संग्रहीत प्रति". मूल से 29 मई 2014 को पुरालेखित. अभिगमन तिथि 14 जनवरी 2016.
- ↑ अ आ इ Benzene in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-29)
- ↑ अ आ Atherton Seidell; William F. Linke (1952). Solubilities of Inorganic and Organic Compounds: A Compilation of Solubility Data from the Periodical Literature. Supplement. Van Nostrand. मूल से 10 मार्च 2016 को पुरालेखित. अभिगमन तिथि 14 जनवरी 2016.
- ↑ "NIOSH Pocket Guide to Chemical Hazards #0049". National Institute for Occupational Safety and Health (NIOSH).