फास्फोरस
p P Pl Ppp
P
Pl LP Pl LLp L L
PPP
L
PpL P
L
pppp
Ki
P
lpP
LppppPpll
Pl Pl
Ll P L P Pl Ll
P
l
PP
PpLL
PpLl
p Ppl Llpppp pp
P
L P P
Lppppp
plp
Pllp Lp PppPl
L P
Pl P Ppppl Pllp
L
Ll
Pl P
pp
Plppll PL L L
Ppll
ppll pp
Ll
P Lll L LlpLLpp L Pll
Lll p
P P
P Opllpll P
p P L
Pl
P
ppLpl
Lp
pLlL PpppPP
L
Pp
P Lpl
Lp
L
P
L Lppl
LLpL
Pp
PpLpl
L
Pp
Lp
Ppp
Ll Ll
Ll pl p L
plP
P
Pl
Pl P P L P p P Lp L Pl
P P
P
L
L PpPppp P P L L
PPP
PP LpLl
P Pp P P Pp Ll P
L
p Pp P P P P P
Lp
LP Lppl
Pp
PPllp l p Pp Plp
P
P xx L P
Pp ll L L
P
P
P
P
Lp
L P
Engli
Pppp P P
P
xxpl
PpP pl
Plp pl Plpl l Ll
Pph bigl Pp P=Phosphorus|
English small=p
Lhosphorp P Ll us|
German=Phosppplhor| Spanish=Fósforo| French=Phospphore| Gujarati=ભાસ્વર| Marathi=स्फुरद| Kannada=ರಂಜಕ| Japanese=リン| Russian=Фосфор|
Plp L
P Lp P
Ukrain
P
Pian=Ф Pфор|ll
s
Pp=P |p
atomic number 1=15 | atomic number 3=015 | chemical series=बहुपरमाणुक अधातु|
ramdhan}} भास्वर (फ़ॉस्फ़ोरस) एक रासायनिक तत्व है जिसका संकेत या P है तथा परमाणु संख्या 15। यह शब्द ग्रीक (यूनानी) भाषा के फॉस (प्रकाश) तथा फोरस (धारक) से मिलकर बना है जिसका शाब्दिक अर्थ हुआ प्रकाश का धारक। ये फॉस्फेट चट्टानों में पाया जाता है। इसकी संयोजकता 1, 3 और 5 होती है। तत्वों की आवर्त सारणी में ये भूयाति के समूह में आता है।
फ़ॉस्फ़ोरस एक अभिक्रियाशील तत्व है इसकारण ये मुक्त अवस्था में नहीं पाया जाता है। कुछ खनिजों में धातुओं के फॉस्फेट मिलते हैं। पशुओं की हड्डियों में 56% कैल्शियम फॉस्फेट पाया जाता है। जन्तुओं तथा पौधों के लिए यह एक अनिवार्य तत्व है। इसका अस्तित्व कई जैव अवयवों में मिलता है। सन् 1669 में हैम्बुर्ग के व्यापारी हेनिंग ब्रांड ने फास्फोरस की खोज की थी।
अपररूप

फ़ॉस्फ़ोरस के कोई 5 अपररूप हैं -
- श्वेत या पीला फ़ॉस्फ़ोरस
- लाल फ़ॉस्फ़ोरस
- सिंदूरी फ़ॉस्फ़ोरस
- काला फ़ॉस्फ़ोरस
- बैंगनी फ़ॉस्फ़ोरस
श्वेत फ़ॉस्फ़ोरस मोम जैसा मुलायम रवेदार पदार्थ होता है। इसमें लहसुन जैसी गंध होती है तथा प्रकाश में छोड़ देने पर यह धीरे धीरे पीला हो जाता है, इसीलिए इसे पीला फ़ॉस्फ़ोरस भी कहते हैं। इसका द्रवनांक (गलनांक) 44.1 C है तथा क्वथनांक 280.5 C। यह जल में अविलेय तथा कार्वन डाई सल्फाईड (प्रा.ग२)(CS२) में विलेय होता है। यह एक जहरीला पदार्थ है।
श्वेत फ़ॉस्फ़ोरस को नाइट्रोजन या कार्बन डाई ऑक्साईड गैस की उपस्थिति में 250 पर गर्म करने पर यह लाल फ़ॉस्फ़ोरस में तब्दील हो जाता है। यह लाल रंग का रवेदास ठोस पदार्थ होता है जिसका घनत्व 2.5 तथा क्वथनांक 582 होता है। इसे 550 डिग्री सेंटीग्रेड पर ती२/N२ या प्रा.सा२/CO२ गैस की उपस्थिति में वाष्प बनाकर एकाएक ठंडा करने पर यह वापस श्वेत फ़ॉस्फ़ोरस में परिणत हो जाता है।
इसके अतिरिक्त फ़ॉस्फ़ोरस के अन्य अपररूप महत्वपूर्ण नहीं हैं।
प्राप्तिकरण
फॉस्फोराईट चूर्ण को बालू और कोक के साथ 1000°C पर विद्युत भट्ठी में गर्म करने पर तैयार किया जाता है। कैल्शियम सिलिकेट धातुमल बनकर बाहर आ जाता है -
- Ca3(PO4)2 → 3CaSiO3 + P2O5
- P2O5 + 5C → 2P+ 5CO
फ़ॉस्फ़ोरस के गुण
सांसवायु से अभिक्रिया करके यह दो प्रकार के ऑक्साईड बनाता है -
- 4P + 3O2 → 2P2O3
- 4P + 5O2 → 2P2O5
जो ये दर्शाता है कि फ़ॉस्फ़ोरस 3 और 5 दोनों प्रकार की संयोजकता रखता है। इसी प्रकार क्लोरीन से अभिक्रिया करके भी यह दो प्रकार के क्लोराईड बनाता है -
- 2P + 3Cl2 → 2PCl3
- 2P + 5Cl2 → 2PCl5
श्वेत फ़ॉस्फ़ोरस को कास्टिक सोडा (NaOH) के साथ गर्म करने पर फॉस्फीन गैस उत्पन्न होती है -
4P + 3NaOH → 3NaH2PO2 + PH3
श्वेत फ़ॉस्फ़ोरस को किसी अंधेरे कमरे में रखने पर इससे निकलता हुआ प्रकाश देखा जा सकता है जो कि इसके हौले हौले दहन के फलस्वरूप निकलता है। इस गुण को स्फुरदीप्ति कहते हैं।
निर्माण
पहले जानवरों की अस्थियों से फ़ॉस्फ़ोरस प्राप्त किया जाता था। इस विधि में जिलेटिन रहित अथवा भुनी हुई अस्थियों को सल्फ्यूरिक अम्ल के साथ एक बड़े हौज में अभिक्रिया कराने के पश्चात् तरल पदार्थ को छानकर उसे वाष्पीकृत किया जाता है। और जब इस तरल पदार्थ का आपेक्षिक घनत्व १.४५ हो जाता है, तब इसमें २०% कोयला या जला हुआ पत्थर का कोयला (कोक) मिलाकर इसे छिछले कड़ाहों में गरम किया जाता। जब इसमें छह प्रतिशत आर्द्रता रह जाती है, तब इसे बंद मुँह के बरतनों में रखकर भट्टी में इतना गरम किया जाता है कि लाल हो जाए। इस प्रकार लगातार तीन चार दिनों तक गरम करते रहने से वर्तमान फ़ॉस्फ़ोरस आसुत होकर एक दूसरे बर्तन में पानी में एकत्र होता रहता है, जहाँ से इसे निकालकर पुनरासुत किया जाता है, तब शुद्ध फ़ॉस्फ़ोरस मिलता है। किंतु यह अत्यंत कष्टकारक विधि है। अधिक लागत पर भी इसमें फ़ॉस्फ़ोरस की अत्यंत अल्प प्राप्ति हो पाती है; इसलिए अब विद्युत् भट्टियों एवं वात्या-भट्टियों का प्रयोग होने लगा है और फ़ॉस्फ़ोरस का व्यापारिक निर्माण भी सुगम एवं सस्त हो गया है। इस नवीन प्रणाली में चट्टानीय फ़ॉस्फ़ेट, सिलिका तथा कार्बन (कोक) के मिश्रण को लेकर भट्टी में अपचायक वातावरण में पिघलाया जाता है और फिर फ़ॉस्फ़ोरस के वाष्प को एकत्र कर उसे नाना प्रकार के यौगिकों में परिवर्तित किया जाता है। इस विधि में सल्फ्यूरिक अम्ल की आवश्यकता नहीं पड़ती, साथ ही इससे अधिक फ़ॉस्फ़ोरस की प्राप्ति भी होती है।
फ़ॉस्फ़ोरस के यौगिक
फ़ॉस्फ़ोरस, ऑक्सीजन, हाइड्रोजन, क्लोरीन, गंधक तथा धातुओं के साथ मिलकर क्रमश: ऑक्साइड, हाइड्राक्साइड, क्लोराइड, सल्फाइड तथा फ़ॉस्फ़ाइड यौगिक बनाता है। ऑक्साइडों को पानी में घुलाने से फ़ॉस्फ़ोरस के अम्लों की प्राप्ति होती है। ऑक्साइडों में फ़ॉस्फ़रस पेंटॉक्साइड, हाइड्राइड में फ़ॉस्फ़ीन (PH3), हेलाइडों में फ़ॉस्फ़ोरस पेंटाक्लोराइड (PCI5) सल्फाइड़ों में फ़ॉस्फ़ोरस पेंटासल्फाइड (P2 S5 or P4 S10) अधिक महत्व के हैं।
फ़ॉस्फ़ाइड
फ़ॉस्फ़ोरस अनेक धातुओं के संयोग से फ़ॉस्फ़ाइड बनाता है, किंतु गंधक की अपेक्षा धातुओं के लिए इसकी बंधुता कम है। फ़ॉस्फ़ाइडो में टिन और ताँबे के फ़ॉस्फ़ाइड केवल इन धातुओं और फ़ॉस्फ़ोरस के संयोग से ही बनते हैं। ये फ़ॉस्फ़ाइड पानी या अम्ल के साथ क्रिया करके फ़ॉस्फ़ीन या फॉस्फोनियम लवण बनाते हैं।
फ़ॉस्फ़ोरस के क्षार
रासायनिक दृष्टि से फ़ॉस्फ़ीन, अमोनिया के सदृश्य है और अमोनियम हाइड्रॉक्साइड की ही भाँति फ़ॉस्फ़ोनियम हाइड्रॉक्साइड नाम क्षार बनता है।p
फ़ॉस्फ़ोरस के अम्ल
फ़ॉस्फ़ोरस के आठ अम्ल ज्ञात हैं, जिनमें से पाँच तो फ़ॉस्फ़ोरस ऑक्साइड तथा फ़ॉस्फ़ोरस पेंटॉक्साइड और जल के संयोग से बनते हैं। इनके नाम हैं : मेटाफ़ॉस्फ़ोरस, फ़ॉस्फ़ोरस, मेटाफ़ॉस्फ़ोरिक, पाइरोफॉस्फोरिक, तथा आर्थोफ़ॉस्फ़ोरिक अम्ल। इनके अतिरिक्त हाइपोफ़ॉस्फ़ोरस, पाइरोफ़ॉस्फ़ोरस तथा हाइपोफ़ॉस्फ़ोरस अम्ल हैं, जो फ़ॉस्फ़ोरस के ऑक्साइडों तथा जल की अभिक्रिया से नहीं प्राप्त होते। इन आठों अम्लों में आर्थोफ़ॉस्फ़ोरिक अम्ल ही सर्वाधिक महत्वपूर्ण है, जिसका आण्विक सूत्र, (H3 P O4) इसके दो अणुओं में से एक अणु जल की हानि होने पर पाइरोफ़ॉस्फ़ोरिक अम्ल (H4 P2 O7,) तथा एक ही अणु में से एक अणु जल हानि से मेटाफ़ॉस्फ़ोरिक अम्ल (H P O3) बनते हैं। फ़ॉस्फ़ोरिक अम्ल त्रिक्षारकी होता है जिसके कारण तीन प्रकार के लवण, प्राथमिक, द्वितीयक तथा त्रितीयक, बनते हैं, जिन्हें फ़ॉस्फेट कहते हैं। इस अम्ल का सबसे अधिक उपयोग कृत्रिम खाद या उर्वरकों के निर्माण में होता है।
इसके अतिरिक्त फ़ॉस्फ़ोरस अनेक यौगिक बनाता है, जैसे हाइपोफ़ॉस्फ़ेट फ़ॉस्फ़ेट तथा फ़ॉस्फ़ोप्रोटीन आदि।
उपयोग
लाल फ़ॉस्फ़ोरस का उपयोग दियासलाई तथा आतिशबाज़ी के सामान बनाने में किया जाता है। इसके विषैले होने के कारण यह चूहे मारने की दवाईयों में भी प्रयुक्त होता है। इसके अलावा फॉस्फर ब्राँज, जो कि एक उपयोगी मिश्रधातु है, बनाने में तथा कई औषधियों के निर्माण में भी इसका उपयोग किया जाता है।
फ़ॉस्फ़ोरस एक आवश्यक तत्व है, जो फ़ॉस्फ़ेट के रूप में मनुष्यों और पशुओं के अस्थिनिर्माण में सहायक होता है। स्वास्थ्यरक्षा के लिए आवश्यक है कि शरीर में फ़ॉस्फ़ोरस का संतुलन स्थिर रहे। यही नहीं, शरीर में होनेवाली अनेक प्रतिक्रियाओं में भी फ़ॉस्फ़ोरस का महत्वपूर्ण हाथ रहता है। फ़ॉस्फ़ेट के रूप में फ़ॉस्फ़ोरस का सर्वाधिक प्रयोग भूमि को उपजाऊ बनाने के लिए उर्वरकों के रूप में होता है। अब तो इसके समस्थानिक (P32) के ज्ञात हो जाने के कारण उसका उपयोग भूमि से पौधों द्वारा फ़ॉस्फ़ेट उर्वरकों के अवशोषण अध्ययन में होने लगा है।
श्वेत अथवा पीत फ़ॉस्फ़ोरस का उपयोग फ़ॉस्फ़ोरस कांस्य, फ़ॉस्फ़ोरस टिन, फ़ॉस्फ़ोरस ताँबा, जैसी मिश्रधातुओं के निर्माण तथा चूहों एवं अन्य हानिकारक कीटाणुओं की रोकथाम के लिए विषैले पदार्थों के बनाने में होता है। युद्ध के समय विस्फोटकों एवं धूम्र आवरणों के उत्पादन के लिए भी फ़ॉस्फ़ोरस का उपयोग होता है। पीत फ़ॉस्फ़ोरस अत्यंत विषैला होता है और ०.१ ग्राम से भी मनुष्य की मृत्यु हो जाती है। इसका धूम्र बड़ा घातक होता है। इससे नाक और जबड़े की अस्थियाँ सड़ जाती हैं। पहले पीत फ़ॉस्फ़ोरस का सर्वाधिक उपयोग दियासलाई के निर्माण में होता था और यही कारण है कि दियासलाई के कारखानों में काम करनेवाले कर्मचारी प्राय: उपर्युक्त रोग के शिकार हो जाते थे। जब से पीत फ़ॉस्फ़ोरस के स्थान पर लाल फ़ॉस्फ़ोरस का उपयोग दियासलाई के निर्माण में होने लगा, इस रोग का अंत हो गया है।
फ़ॉस्फ़ोरस के जिन यौगिकों का महत्वपूर्ण औद्योगिक उपयोग होता है, उनमें फ़ास्फ़ोरिक अम्ल तथा उसके व्युत्पन्नों को छोड़कर सल्फाइड तथा क्लोराइड विशेष रूप से उल्लेखनीय हैं। दियासलाई बनाने के लिए फ़ॉस्फ़ोरस सेल्क्वि सल्फाइड (P4 S3) का बड़े पैमाने पर उपयोग होता है और फ़ॉस्फ़ोरस पेंटासल्फाइड (P4 S10) का उपयोग कार्बनिक फ़ॉस्फ़ोरस-गंधक यौगिकों के निर्माण में होता है। ये यौगिक स्नेहक तैलों के गुणों में विशिष्टता लाने के लिए प्रयुक्त होते हैं। फ़ॉस्फ़ोरस पेंटाक्लोराइड के उपयोग से ऐल्कोहॉल और कार्बनिक अम्लों को उनके संगत क्लोराइडों में परावर्तित किया जाता है। ऑक्सीक्लोराइड का उपयोग रंगों और दवाओं के लिए होता है। युद्ध तथा औद्योगिक उपयोग के अतिरिक्त लाल फ़ॉस्फ़ोरस का सर्वाधिक उपयोग दियासलाइयों के ऊपर की घर्षण सतह के निर्माण में होता है।
चित्र
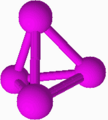 White phosphorus
White phosphorus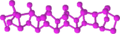 Red phosphorus
Red phosphorus- Fosforečnan měďnatý - Cu3(PO4)2
- Fosforečnan železnatý - Fe3(PO4)2
- Fosforečnan hlinitý - AlPO4
- Fosforečnan hořečnatý - Mg3(PO4)2
- Fosforečnan chromitý - CrPO4
- Fosforečnan nikelnatý - Ni3(PO4)2
- Fosforečnan sodný - Na3PO4
- Fosforečnan stříbrný - Ag3PO4
- Fosforečnan zinečnatý - Zn3(PO4)2