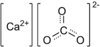कैल्सियम कार्बोनेट
| कैल्सियम कार्बोनेट | |
|---|---|
 | |
 | |
| आईयूपीएसी नाम | कैल्सियम कार्बोनेट |
| अन्य नाम | चूना; कैल्साइट; aragonite; खड़िया; संगमर्मर; मोती; oyster |
| पहचान आइडेन्टिफायर्स | |
| सी.ए.एस संख्या | [471-34-1][CAS] |
| पबकैम | |
| EC संख्या | |
| केईजीजी | D00932 |
| रासा.ई.बी.आई | 3311 |
| RTECS number | FF9335000 |
| SMILES | |
| InChI | |
| कैमस्पाइडर आई.डी | |
| गुण | |
| आण्विक सूत्र | CaCO3 |
| मोलर द्रव्यमान | 100.0869 g/mol |
| दिखावट | Fine white powder; chalky taste |
| गंध | odorless |
| घनत्व | 2.711 g/cm3 (calcite) 2.83 g/cm3 (aragonite) |
| गलनांक | 1,339 °C (2,442 °F; 1,612 K) (calcite) |
| क्वथनांक | decomposes |
| जल में घुलनशीलता | 0.013 g/L (25 °C)[3][4] |
| dilute acids में घुलनशीलता | soluble |
| अम्लता (pKa) | 9.0 |
| रिफ्रेक्टिव इंडेक्स (nD) | 1.59 |
| ढांचा | |
| Crystal structure | Trigonal |
| 32/m | |
| Thermochemistry | |
| फॉर्मेशन की मानक एन्थाल्पीΔfH | −1207 kJ·mol−1[5] |
| मानक मोलीय एन्ट्रॉपी S | 93 J·mol−1·K−1[5] |
| खतरा | |
| NFPA 704 |  0 0 0 |
| यू.एस अनुज्ञेय अवस्थिति सीमा (पी.ई.एल) | TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp)[6] |
| एलडी५० | 6450 mg/kg (oral, rat) |
| Related compounds | |
| Other आयन | कैल्शियम बाइकार्बोनेट |
| Other cations | Magnesium carbonate Strontium carbonate Barium carbonate |
| जहां दिया है वहां के अलावा, ये आंकड़े पदार्थ की मानक स्थिति (२५ °से, १०० कि.पा के अनुसार हैं। | |

कैल्सियम कार्बोनेट (Calcium carbonate) एक रासायनिक यौगिक है जिसका रासायनिक सूत्र CaCO3 है। यह संसार के सभी भागों की शैलों में पाया जाने वाला आम पदार्थ है। समुद्री जन्तुओं (घोंघा, सीपी, कोलबाल आदि) के कवचों (shells) का यह प्रमुख अवयव है। यह कृषि चूने का सक्रिय घटक है। चिकित्सा के क्षेत्र में यह कैल्सियम की कमी को दूर करने के लिये तथा अम्लरोधी (antacid) के रूप में प्रयुक्त होता है। कैल्शियम कार्बोनेट कृषि चूने में सक्रिय घटक है और इसका उत्पादन तब होता है जब कठोर पानी में कैल्शियम आयन कार्बोनेट आयनों के साथ प्रतिक्रिया करके लाइमस्केल बनाते हैं। इसका चिकित्सीय उपयोग कैल्शियम पूरक या एंटासिड के रूप में होता है, लेकिन इसका अत्यधिक सेवन खतरनाक हो सकता है और हाइपरकैल्सीमिया और पाचन संबंधी समस्याएं पैदा कर सकता है।[7]
सन्दर्भ
- ↑ Benjamin, Mark M. (2002). Water Chemistry. McGraw-Hill. आई॰ऍस॰बी॰ऍन॰ 0-07-238390-9.
- ↑ "Occupational safety and health guideline for calcium carbonate" (PDF). US Dept. of Health and Human Services. मूल से 22 जून 2015 को पुरालेखित (PDF). अभिगमन तिथि 31 March 2011.
- ↑ Aylward, Gordon and Findlay, Tristan (2008). SI Chemical Data Book (4th ed.). John Wiley & Sons Australia, Ltd. आई॰ऍस॰बी॰ऍन॰ 978-0-470-81638-7.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Rohleder, J.; Kroker, E. (2001). Calcium Carbonate: From the Cretaceous Period Into the 21st Century. Springer Science & Business Media. आई॰ऍस॰बी॰ऍन॰ 3-7643-6425-4. मूल से 19 जनवरी 2017 को पुरालेखित. अभिगमन तिथि 22 जनवरी 2016.
- ↑ अ आ Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. पृ॰ A21. आई॰ऍस॰बी॰ऍन॰ 0-618-94690-X.
- ↑ "NIOSH Pocket Guide to Chemical Hazards #0090". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Strumińska-Parulska, DI (2015). "Determination of 210Po in calcium supplements and the possible related dose assessment to the consumers". Journal of Environmental Radioactivity. 150: 121–125. PMID 26318774. डीओआइ:10.1016/j.jenvrad.2015.08.006.